Galerie der Bilder von 2021
Februar 2021
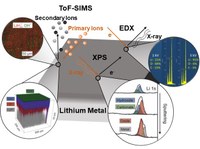
Eingehende Charakterisierung von Lithiummetalloberflächen: Die Verwendung von Lithiummetall als Anode wird intensiv untersucht, um die Energiedichte von zukünftigen Batterien signifikant zu erhöhen. Aufgrund seiner hohen Reaktivität ist Lithium nativ mit einer Passivierungsschicht bedeckt, die den Einsatz in der Batterie beeinflusst. Diese Passivierungsschicht wird jedoch meist nicht berücksichtigt und charakterisiert. Vor diesem Hintergrund haben wir verschiedene Lithiumproben systematisch mit Röntgenphotoelektronen-spektroskopie (XPS), Flugzeit-Sekundärionen-Massenspektrometrie (ToF-SIMS) und komplementärer energiedispersiver Röntgenspektroskopie (EDX) charakterisiert, um ein vollständiges drei-dimensionales chemisches Bild der Oberflächenpassivierungsschicht zu erhalten. Außerdem haben wir mögliche Faktoren, die die Passivierungsschicht beeinflussen, sowie das experimentelle Vorgehen, das erforderlich ist, um einen hochreaktiven Analyten wie Lithium zuverlässig zu charakterisieren, untersucht. (Bild eingereicht von Svenja Otto.)
Anzeigen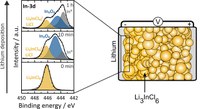
März 2021
Feststoffbatterien werden derzeit aufgrund ihrer im Vergleich zu Lithium-Ionen-Batterien besseren Eigenschaften wie einer höheren Sicherheit oder breiteren Betriebstemperatur und vergleichbaren ionischen Leitfähigkeiten intensiv erforscht und charakterisiert. Um die höhere Dichte der Festelektrolyte auszugleichen, ist die Verwendung von Lithiummetall als Anodenmaterial nötig, um gute gravimetrische und volumetrische Energiedichten zu erhalten. Lithiummetall ist jedoch sehr reaktiv. Entstehen bei der Reaktion des Festelektrolyten mit Lithium elektronisch leitfähige Produkte, kann dieser Elektrolyt nicht in direktem Kontakt mit Lithium verbaut werden, da es sonst zu Kurzschlüssen kommen kann. Um die Reaktionsprodukte des Festelektrolyten Li3InCl6 mit Lithium zu untersuchen, wird mittels Sputterdeposition Lithium auf den Elektrolyten aufgebracht und durch in situ Röntgen-Photoelektronenspektroskopie (XPS) untersucht, welche Produkte entstehen. Es zeigt sich, dass Li3InCl6 u.a. in In2O3 und Indiummetall zersetzt wird. Da Indiummetall elektronisch leitfähig ist, zersetzt sich der Elektrolyt so lange bis entweder Li3InCl6 oder das Lithium aufgebraucht sind, kann der Elektrolyt nicht in direktem Kontakt mit Lithium verwendet werden. (Bild eingereicht von Luise Riegger)
Anzeigen