Arbeitsgruppe Olias
Comparative Protozoan Pathobiology
Click here for information in English.
Parasiten aus dem Stamm der Apicomplexa sind Krankheitserreger, die für bedeutende Krankheiten bei Mensch und Tier verantwortlich sind, darunter Malaria, Toxoplasmose, Cryptosporidiose und Theileriose. In unserer Gruppe interessieren wir uns für die Mechanismen, durch die diese intrazellulären Parasiten mit ihren Wirtszellen interagieren und Krankheiten verursachen.
Im Labor konzentrieren wir uns auf die Zoonoseerreger Toxoplasma und Cryptosporidium sowie Theileria. Ein besseres Verständnis der zellbiologischen und molekularen Grundlagen, die an der Parasit-Wirt-Interaktion beteiligt sind, kann die Entwicklung neuer Therapeutika ermöglichen und die schwerwiegenden gesundheitlichen und sozioökonomischen Auswirkungen dieser Krankheitserreger reduzieren.
Etwa ein Viertel der Weltbevölkerung ist mit Toxoplasma infiziert. Zoonotische Infektionen können eine Vielzahl schwerwiegender klinischer Folgen haben, wie eine Enzephalitis oder kongenitale Toxoplasmose während der Schwangerschaft.
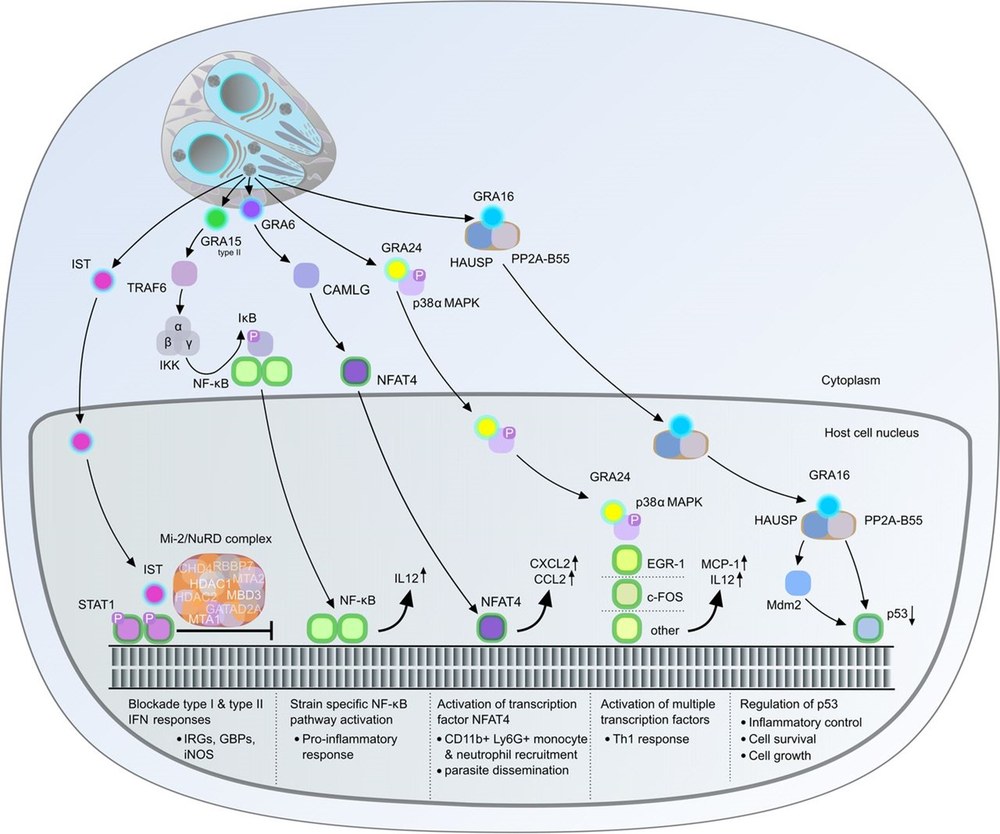
Abbildung 1: Sekretierte Effektorproteine von Toxoplasma wie IST verändern die Signaltransduktion der infizierten Wirtszelle. Publikation: https://pubmed.ncbi.nlm.nih.gov/28404792/
Die Cryptosporidiose hingegen ist eine Durchfallerkrankung des Menschen, die vor allem Kinder und immungeschwächte Personen gefährdet. Cryptosporidium-Parasiten gehören zu den häufigsten Erregern von Durchfallerkrankungen bei Kindern und sind mitverantwortlich für die hohe Kindersterblichkeit im Globalen Süden. Cryptosporidien sind auch eine der Hauptursachen für schwere und oft tödliche Durchfallerkrankungen bei Kälbern und anderen Jungtieren.
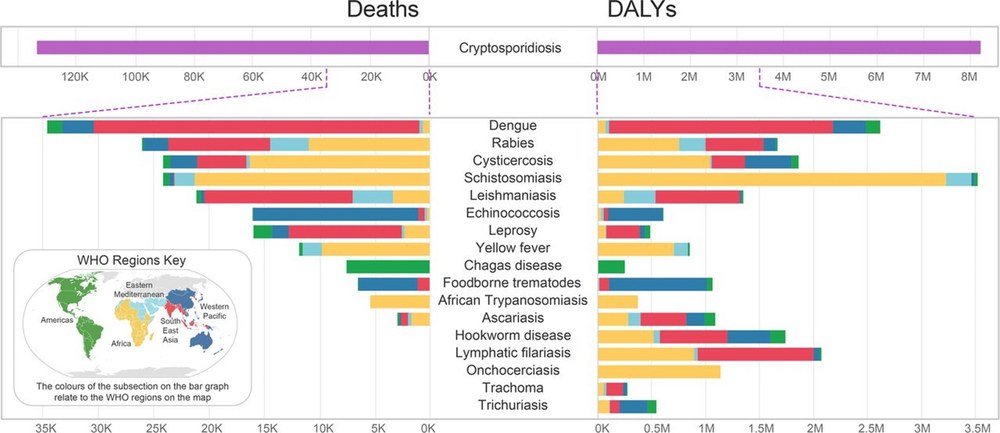
Abbildung 2: Geschätzte 133.000 Todesfälle pro Jahr und 8.200.000 DALYs durch Cryptosporidiose (oben), die weit über die NTDs der WHO hinausgehen (siehe Unterschiede in der Skalierung). DALYs, disability-adjusted life years, Maß zur Quantifizierung der Krankheitslast; NTDs, vernachlässigte Tropenkrankheiten. Publikation: https://pubmed.ncbi.nlm.nih.gov/37541693/
Die Theileriose ist eine Rinderkrankheit mit großen sozioökonomischen Auswirkungen in Afrika südlich der Sahara und in Asien. Theileria-Parasiten sind die einzigen eukaryotischen Krankheitserreger, die ihre Wirtszelle vollständig transformieren können. Es wird vermutet, dass ihre Transformationsfähigkeit durch die Störung mehrerer Signaltransduktionswege ermöglicht wird, wodurch die Wirtszellen in einen proliferativen und unsterblichen, krebsähnlichen Zustand versetzt werden.
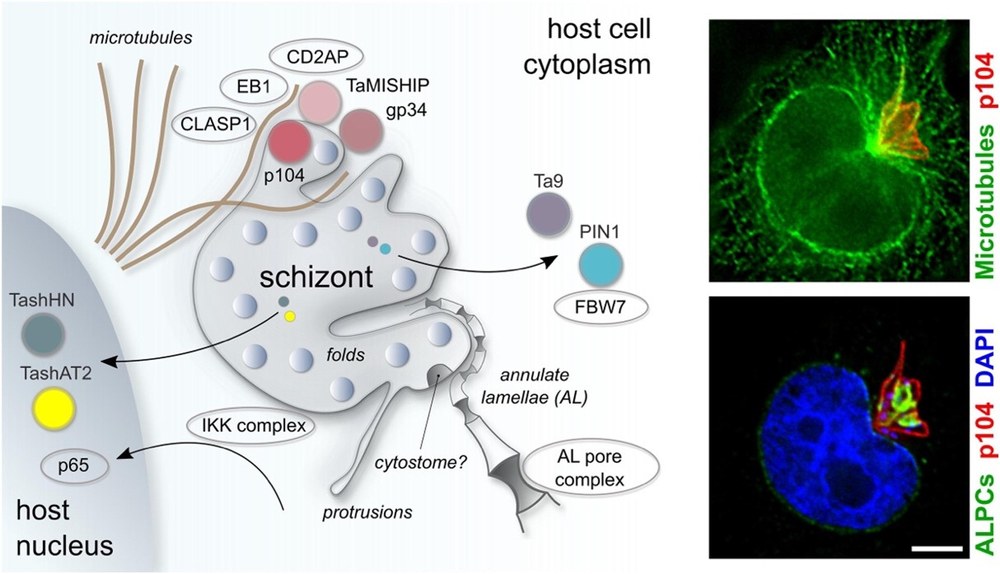
Abbildung 3: Schematische Darstellung der wichtigsten Wirt-Parasit-Interaktionen in mit Theileria annulata infizierten Leukozyten. Publikation: https://pubmed.ncbi.nlm.nih.gov/33959614/
