AG Dr. Daniel Schröder
- Aktueller Hinweis
-
Ab dem 01.04.2021 sind wir an der TU Braunschweig zu finden: https://www.tu-braunschweig.de/ines/
- AG Dr. Daniel Schröder
-
Willkommen auf den Seiten der Arbeitsgruppe Schröder!MOOSE = Metall und O2: Synergie durch Elektrochemie
 FIB-REM-Aufnahme einer Kathode für Zink-Sauerstoff-Batterien(B. Luerßen, B. Mogwitz, D. Stock)
FIB-REM-Aufnahme einer Kathode für Zink-Sauerstoff-Batterien(B. Luerßen, B. Mogwitz, D. Stock)
- Ausgewählte Ergebnisse aus dem Labor
Dezember 2020
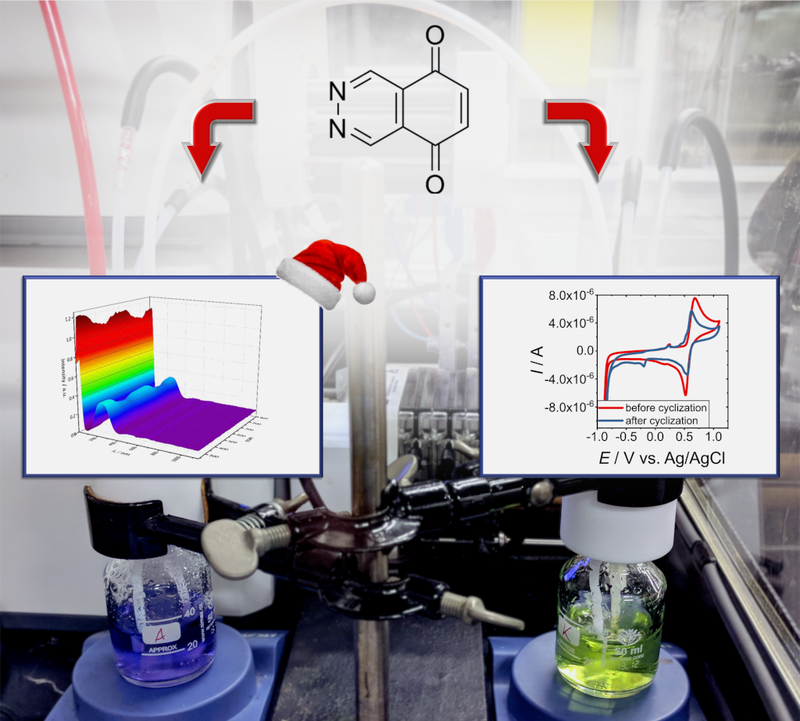
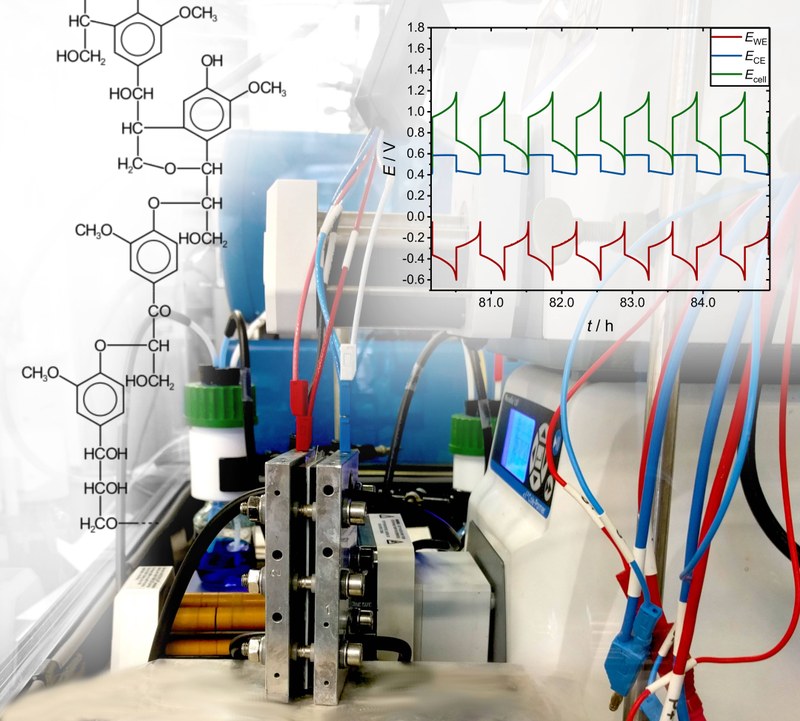
Organische Redox-Flow-Batterien (RFB) rückten in den letzten Jahren verstärkt in den Fokus als Großenergiespeicher, da diese im Vergleich zu der etablierten Vanadium-RFB keine toxischen und seltenen Metallionen enthalten. Aufgrund dessen, steigt die Nachfrage an neuen organischen Aktivmaterialien, welche als Katholyt oder Anolyt in der organischen RFB eingesetzt werden. Die Langzeitstabilität der organischen Aktivmaterialien ist dabei maßgeblich für einen möglichen kommerziellen Erfolg der RFB. Unsere Arbeitsgruppe beschäftigt sich hierbei mit der Charakterisierung der Leistungsfähigkeit und der Stabilität organischer Aktivmaterialien für RFB im Betrieb. Im Bild sind beispielhaft die erzielten Ergebnisse mit einem Diazanaphthochinon (synthetisiert durch die AG Wegner; Kooperation im Rahmen einen vom BMEL geförderten Projektes) gezeigt. Das Diazanaphthochinon (oben) wurde mit Hilfe einer operando UV/Vis-Zelle vermessen (links), während gleichzeitig elektrochemische Messungen (rechts) durchgeführt wurden. Die UV/Vis-Messungen dienen hierbei zur Identifikation von Produkten und Degradationsprodukten, wohingegen es elektrochemische Langzeitmessungen ermöglichen die Kinetik der auftretenden Degradationsreaktionen zu bestimmen. Insgesamt setzt unsere Arbeitsgruppe stets auf eine schlagkräftige Kombination aus Analytik (operando, in-situ und ex-situ) sowie theoretischen Betrachtungen, um das Verständnis der organischen Aktivmaterialien für RFB zu erweitern. (Bild eingereicht von: Dominik Emmel und Simon Kunz)
Oktober 2020
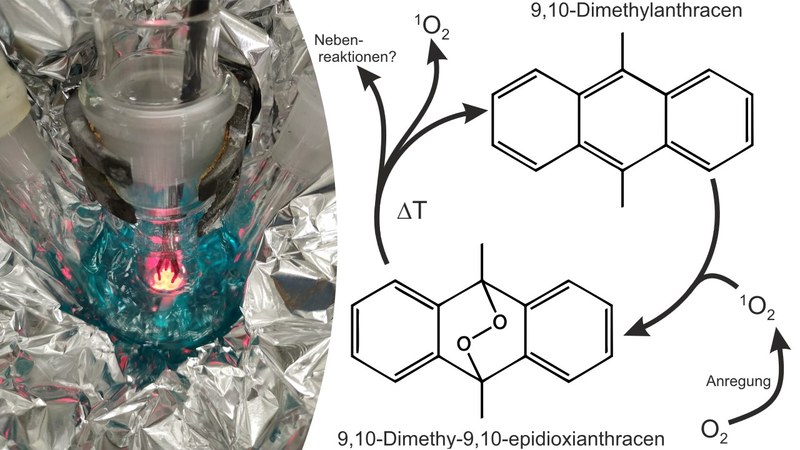
Lithium-Sauerstoff-Batterien gelten auf Grund ihrer hohen theoretischen Speicherkapazität als mögliche Energiespeicher der Zukunft, sowohl für mobile als auch stationäre Anwendungen. In ihnen wird metallisches Lithium (Anodereaktion) mit Sauerstoff (Kathodenreaktion) zu Lithiumperoxid umgewandelt. Das gebildete Lithiumperoxid wird in der Batterie gespeichert und beim Laden wieder in Sauerstoff und metallisches Lithium umgewandelt. Trotz intensiver Forschung in den letzten Jahren können mit diesem Batterietyp derzeit noch keine hohen Zyklenzahlen für das elektrische Wiederaufladen erreicht werden. Als Ursache hierfür gelten verschiedene Nebenreaktionen beim Lade- und Entladevorgang, deren Ursprung bisher nicht vollständig aufgeklärt werden konnte. Eine mögliche Quelle für die ungewollt entstehenden Nebenprodukte ist der während des Betriebs gebildete Singulett-Sauerstoff (¹O₂). Bei ¹O₂ handelt es sich um eine angeregte, kurzlebige Variante von molekularem Sauerstoff. Sie ist ein sehr gutes Oxidationsmittel und reagiert mit den anderen Komponenten der Batterie wie dem Elektrolyten und den Elektrodenmaterialien. Da ¹O₂ aber nicht langzeitstabil ist und bereits nach wenigen Millisekunden abreagiert, ist der Nachweis schwierig. Eine Möglichkeit zum Nachweis ist das sogenannte Trapping bei dem ¹O₂ mit anderen Molekülen zur Reaktion gebracht wird, welche dann später nachgewiesen werden können. In der AG Schröder wird derzeit das in der Abbildung gezeigte Molekül 9,10-Dimethylanthracen (DMA) als Nachweismittel für 1O2 in Lithium-Sauerstoff-Batterien untersucht, da es spezifisch mit Singulett-Sauerstoff zu 9,10-Dimethyl-9,10-epidioxianthracen reagiert (DMA-O₂). Über dessen Stabilität und den Einfluss auf die Chemie von Lithium-Sauerstoff-Batterien ist bisher wenig bekannt. Das dafür benötigte DMA-O₂ wird in der AG Schröder photochemisch hergestellt (siehe Bild) und anschließend aufgereinigt bevor es weiter untersucht wird. (Bild eingereicht von: Adrian Schürmann)
Juli 2020
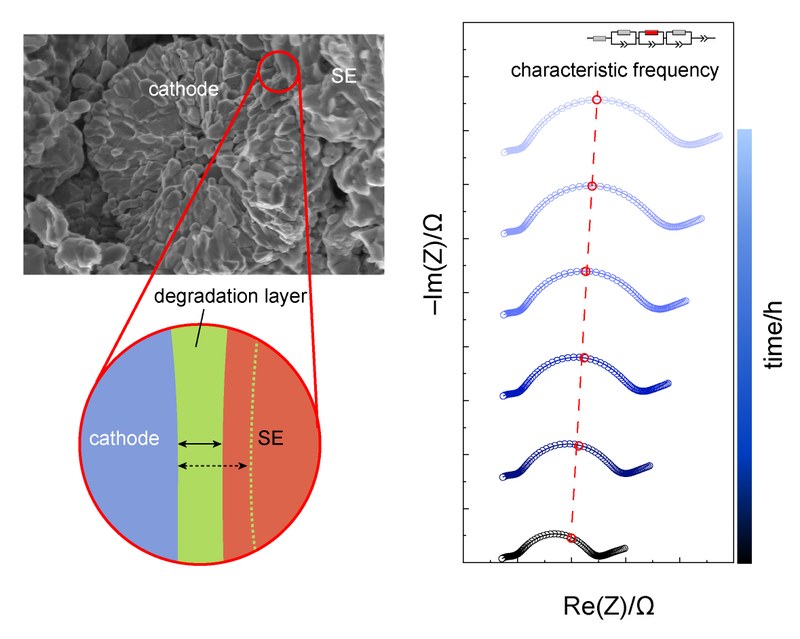
Lithium-Ionen-Batterien (LIBs) erfreuen sich derzeit großer Beliebtheit. Kommerziell erhältliche LIBs zeichnen sich jedoch auch unter Umständen durch gravierende Sicherheitsprobleme aus, die sich aus der Entflammbarkeit des organischen Flüssigelektrolyten ergeben. Um dieses Sicherheitsrisiko zu umgehen, werden derzeit Festkörperbatterien (SSBs) als vielversprechende Ergänzung zu Batterien mit organischem Flüssigelektrolyte diskutiert. Allerdings steht die Entwicklung von SSBs noch vor beträchtlichen Herausforderungen, die eine schnelle Kommerzialisierung verhindern. Eine der Hauptherausforderungen ist der hohe Ladungstransferwiderstand zwischen den Elektrodenmaterialien und dem Festelektrolyten aufgrund der instabilen Grenzfläche zwischen Elektrode und Elektrolyt. Daher untersuchen die AG Schröder und die AG Janek gemeinsam die zugrundeliegenden Degradationsprozesse in SSBs. Im Detail beschäftigen wir uns mit den Degradationsreaktionen an der Grenzfläche zwischen verschiedenen Kathodenmaterialien und Festelektrolyten – dies im Rahmen des DE-JPN-Verbundprojektes InCa, welches vom BMBF gefördert wird. Das REM-Bild zeigt die verwendeten Kathodenpartikel und den Festelektrolyten; die Grafik veranschaulicht den Degradationsvorgang an der Grenzfläche. Hierzu wurden Impedanzmessungen durchgeführt, um den Einfluss der Degradation auf den Grenzflächenwiderstand mit zunehmender Alterungszeit zu verfolgen. Eine charakteristische Frequenz (~200 – 500 Hz), die den Prozessen während der Degradation an der Grenzfläche zugeordnet werden kann, ist entsprechend im Nyquist-Diagramm eingezeichnet. (Bild eingereicht von TongTong Zuo und Daniel Schröder).
März 2020
Die Kommerzialisierung von reinen Metallen als Anodenmaterial wird im Rahmen der Batterieforschung oftmals als „Heiliger Gral“ bezeichnet. Diese Aussage beruht darauf, dass die Energiedichte von Batterien durch die Verwendung von reinen Metallen deutlich erhöht werden kann. Jedoch müssen noch verschiedene Herausforderungen vor der Kommerzialisierung von Metallanoden bewältigt werden. Eine der Hauptherausforderungen ist das Wachstum von sogenannten Dendriten während des Ladens der Batterie zu verhindern. Die AG Schröder hat sich im Rahmen mehrerer Studienprojekte mit der Analyse des dendritischen Wachstums und der Verhinderung dessen beschäftigt. In ihrer Bachelorthesis hatte Ronja Haas das Wachstum von Dendriten durch den Einsatz von verschiedenen Natrium-Metall-Legierungen vermindert. Hierzu verwendete sie zum einen flüssige Natrium-Kalium-Legierungen als Anode und zum anderen Natrium-Zinn-Legierungen als Schutzschicht. Auch im Rahmen seiner Masterthesis befasste sich Julian Kreissl mit der Verhinderung von Dendriten in Natrium-Sauerstoff-Batterien. In Kooperation mit der Arbeitsgruppe von Prof. Dr. Peter R. Schreiner setzte er funktionalisierte Diamantoide als Additiv im Elektrolyten. Diese „molekularen Diamanten“ werden während des Ladens in die Anode eingebaut und sorgen für eine planare Metallabscheidung (Abbildung a; 10.1002/cssc.201903499). Beide Arbeiten wurden im Zuge des studentischen Nachwuchsprogramms für Elektromobilität des Bundesministeriums für Bildung und Forschung (BMBF) und der Fraunhofer-Gesellschaft, DRIVE-E, in den Kategorien „Beste Bachelorarbeit“ und „Beste Masterarbeit“ mit dem jeweils ersten Platz ausgezeichnet (Abbildung b; https://www.uni-giessen.de/ueber-uns/pressestelle/pm/pm188-19driveepreisfuerwissenschaftlichennachwuchs ; https://www.iisb.fraunhofer.de/en/press_media/press_releases/pressearchiv/archiv_2019/drive-e_2019_studienpreise.html).
Juli 2019
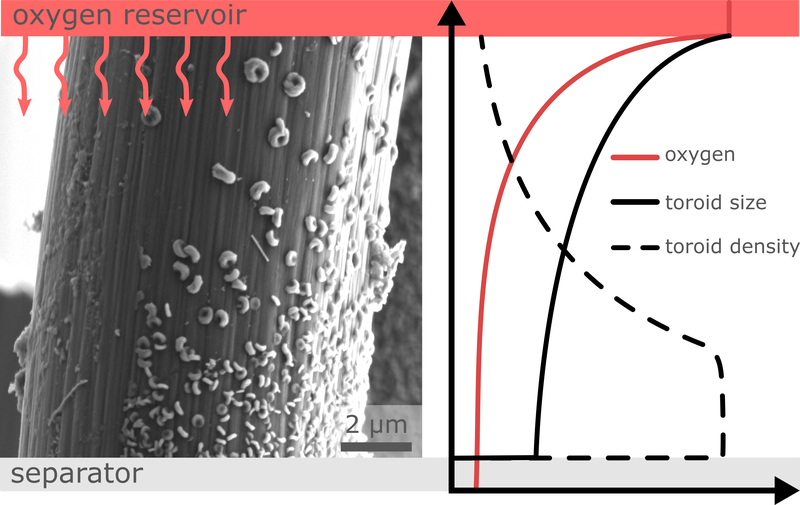
Wiederaufladbare Metall-Sauerstoff-Batterien gelten als eine mögliche Technologie für den Einsatz in zukünftigen Energiespeichern. Besonders Alkalimetall-Sauerstoff-Batterien, wie zum Beispiel Lithium-Sauerstoff-Batterien, stehen vor allem wegen ihrer hohen theoretischen Energiedichte im Fokus von Industrie und Forschung. Da das während des Entladens gebildete Lithiumperoxid als Feststoff an der Kathodenstruktur ausfällt, spielen das Kathodendesign und das Verständnis über den Wachstumsmechanismus eine entscheidende Rolle, um eine maximale Energiedichten zu erzielen. Aus diesem Grund wird im BMBF-Verbundprojekt MeLuBatt – in enger Zusammenarbeit mit dem Institut für Energie- und Systemverfahrenstechnik (InES) der TU Braunschweig und dem Fraunhofer-Institut für Fertigungstechnik und Angewandte Materialforschung (IFAM) in Oldenburg – derzeit das Wachstumsverhalten des Entladeprodukts in der Kathode von Lithium-Sauerstoff-Batterien untersucht. Das REM-Bild zeigt eine vergrößerte Kohlenstofffaser der Kathode, auf der sich toroidähnliche Li2O2-Partikel gebildet haben. Die Größe und Partikeldichte dieser Toroide ist dabei stark von der Verfügbarkeit an gelöstem Sauerstoff im Elektrolyten abhängig: Bei größerer Sauerstoffverfügbarkeit (auf der O2-Reservoirseite; oben im Bild) werden wenige, dafür aber deutlich größere Toroide gebildet, während tiefer im Elektrolyten (auf der Separatorseite; unten im Bild) die Toroide kleiner sind, jedoch in einer größeren Dichte aufwachsen. Das Diagramm verdeutlicht schematisch, wie die Größe und Dichte der Toroide von der O2-Verfügbarkeit im Elektrolyten, entlang einer Kohlenstofffaser, abhängen. (Bild eingereicht von Julian Kreißl, Daniel Langsdorf und Daniel Schröder).
November 2018
Redox-Flow-Batterien eignen sich für die stationäre Zwischenspeicherung der durch regenerative Energieträger bereit gestellten und aufgrund von Umwelteinflüssen fluktuierenden Energie. Der spezielle Aufbau der Redox-Flow-Batterie ermöglicht es hierbei, die Energie in Form von flüssigen Elektrolyten unterschiedlicher Oxidationsstufen außerhalb der eigentlichen elektrochemischen Zelle zu speichern. Bei aktuellem Stand der Technik stellt das Aktivmaterial im Elektrolyten den Hauptkostenfaktor von Redox-Flow-Batterien dar. Zur effektiven Reduzierung der Herstellungs- und Betriebskosten sollen daher künftig kostengünstige organische Moleküle, die beispielsweise durch die Aufbereitung von Abfallprodukten aus der Zellstoffindustrie gewonnen werden könnten, als Aktivmaterial in Redox-Flow-Batterien eingesetzt werden.Auf der Suche nach potentiellen Zielmolekülen für diese Anwendung werden derzeit im BMEL-Projekt FOREST geeignete organische Verbindungen auf ihre Stabilität und Leistungsfähigkeit getestet. Das Bild zeigt den verwendeten Messaufbau für eine Redox-Flow-Batterie im Labormaßstab (Mitte). Die gelösten Aktivmaterialien – hier in Form eines organischen Elektrolyten auf der Anoden- und eines Vanadium(IV)-basierten Elektrolyten auf der Kathodenseite – werden mittels Pumpen in die Batterie befördert. Eine Referenzelektrode ermöglicht es, während der Zyklisierung der Batterie die Potentiale der Arbeits- (WE) und Gegenelektrode (CE) aufzuzeichnen und infolge dessen Rückschlüsse auf die Leistungsfähigkeit und das Degradationsverhalten der Aktivmaterialien zu ziehen (rechts).Bild eingereicht von Dominik Emmel und Jonas Hofmann, AG Dr. Daniel Schröder
Februar 2018
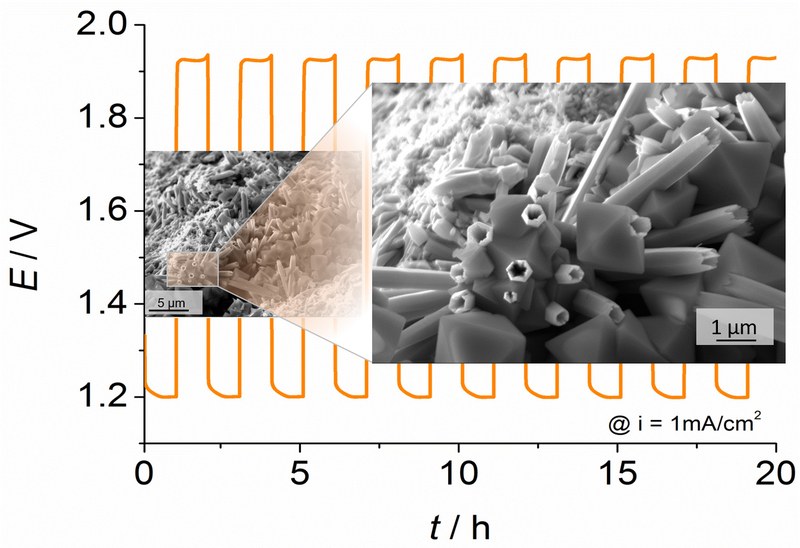
Erhalten wir in elektrisch aufladbaren Zink–Luft Batterien wirklich immer nur ZnO als Entladeprodukt? Metall–Luft Batterien gelten heute als eine gute Alternative, um Energie zwischenzuspeichern. Dabei ist vor allem die Zn/Luft-Batterie aufgrund von geringen Herstellungskosten, Wiederverwendbarkeit und Sicherheit ein aussichtsreicher Kandidat. Aus diesem Grund steht die Entwicklung einer wiederaufladbaren Zn/Luft-Batterie in den letzten Jahren im Fokus der Forschung, und intensive Forschungsanstrengungen wurden unternommen, um ihre Zyklenstabilität zu erhöhen.Ein Schlüsselproblem der alkalischen elektrisch wiederaufladbaren Zn/Luft-Batterie ist die elektrochemische Reaktion an der Zn-Elektrode: Das Entladeprodukt ZnO kann nicht vollständig in Zn umgewandelt werden. In Allgemeinen wird die Bildung von ZnO durch eine Vielzahl an Parametern wie lokale Konzentrationsunterschieden, den pH-Wert und Diffusion von Zn-Ionen in der alkalischen Lösung beeinflusst. In einer elektrisch wiederaufladbaren Zn/Luft-Batterie werden die Keimbildung und das Wachstum von ZnO jedoch darüber hinaus auch vom Zusammenspiel zwischen Entlade- und Ladeprozess gelenkt.Wir haben herausgefunden, dass auch Batteriekomponenten, wie beispielsweise ein Stromabnehmer aus Zinn, die Art des Entladeprodukts während der Zellzyklisierung beeinflussen können. Die Rasterelektronenmikroskop-Aufnahme zeigt orthorhombische ZnSnO3- und Zn2SnO4-Kristallite umgeben von hexagonalen ZnO-Röhren, die wir nach 25 Zyklen auf der Oberfläche der Zn-Elektrode beobachtet haben. Diese und weitere Untersuchungen sind Teil des Deutsch-Japanischen BMBF-Kooperationsprojektes „Zisabi“, um einen vertieften Einblick in die Prozesse der wiederaufladbaren Zn/Luft-Batterie zu erhalten. (Bild eingereicht von Saustin Dongmo und Daniel Schroeder.)
Oktober 2017
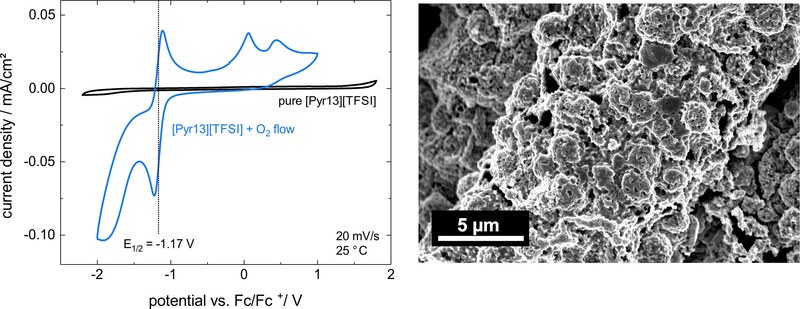
Die elektrochemische Synthese aus Ionischen Flüssigkeiten (ILs) bietet eine Alternative auf dem Weg zu ungewöhnlichen Edelmetallverbindungen, da bei dieser Route auf extreme Bedingungen (hohe Drücke oder Temperaturen, reaktive und gesundheits-/umweltgefährdende Edukte) verzichtet werden kann. Hierbei wird analog zu den Reaktionen in Metall-Luft-Zellen Sauerstoff an einer Kathode zum Superoxid reduziert (Red1: O2 + e– → O2–), Silber an der Anode oxidiert (Ox: Ag → Ag+ + e–) und diese können gemeinsam zu einem Silberoxid AgxOy ausfallen bzw. weiter disproportionieren. Die bei Ox entstehenden Metallkationen konkurrieren allerdings mit dem gelösten Sauerstoff an der Kathode um die Reduktion. Somit kann an der Kathode statt Red1 auch die umgekehrte Reaktion zu Ox ablaufen (Red2: Ag+ + e– → Ag) und die Sauerstoffreduktion unterdrückt werden.Sättigt man die IL ([Pyr13][TFSI]) mit Sauerstoff ist das Sauerstoffreduktionssignal bei einem Potential von -1,17 V (Red1) im Zyklovoltammogramm sichtbar (linke Abbildung, blaue Kurve). Fügt man nun Silbersalz (Ag[TFSI]) hinzu und hat somit Silber und Sauerstoff gleichzeitig in Lösung vorliegen, verschiebt sich das Halbwellen-Potential auf -0,38 V. Dies entspricht nahezu dem des Silberredoxpotentials (-0,4 V). Somit findet (im Gegensatz zu den Reaktionen in Metall-Luft-Zellen) unter diesen Bedingungen keine Reaktion von Sauerstoff mit Silber zum Metalloxid statt (Red1 und Ox), sondern reines Silber wird abgeschieden und der Sauerstoff bleibt unbeteiligt (Red2 und Ox). Eine REM-Aufnahme der porösen Morphologie des abgeschiedenen Silbers ist rechts dargestellt.Ziel des Projekts ist den Einfluss diverser Parameter (Temperatur, CV Scangeschwindigkeit, Potential, Konzentrationen) auf das Auftreten der konkurrierenden Reduktionsreaktionen Red1 bzw. Red2 zu untersuchen und so ein besseres Verständnis für die auftretenden Reaktionen zu erhalten. (Bild eingereicht von Peter Schmitz)
Oktober 2016
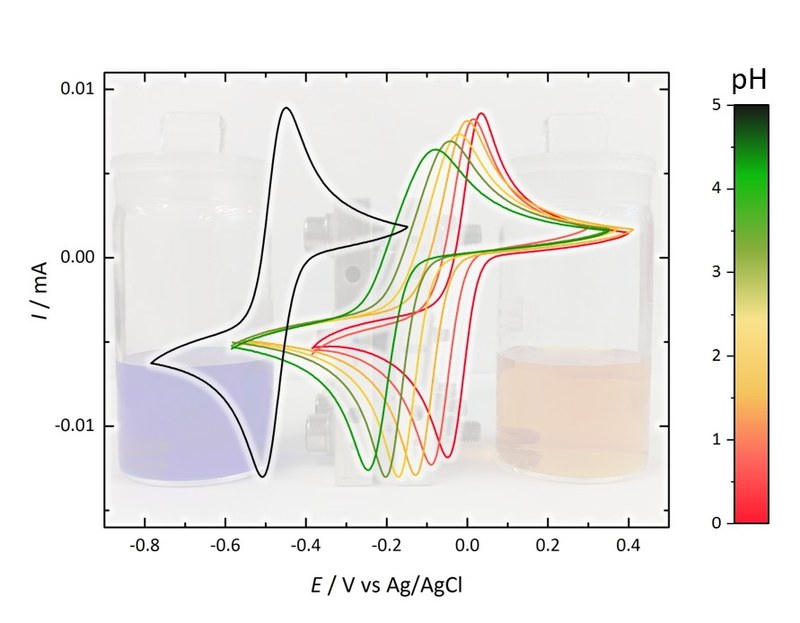
Vor dem Hintergrund der Etablierung alternativer Energieträger gewinnen verschiedene Arten der stationären Energiespeicherung stetig an Relevanz. Fernab konventioneller Batteriesysteme wie der Lithium-Ionen-Batterie geraten dabei alternative Speicherlösungen in den Fokus, deren Komponenten idealerweise kostengünstig und nachhaltig zu erschließen sind. So können beispielsweise organische Moleküle, welche aus verschiedensten Rohstoffen gewonnen werden können, für den Einsatz in elektrochemischen Zellen optimiert werden. Die für diese Anwendung geeigneten Zielmoleküle werden durch eine Kooperation zwischen dem Physikalisch-Chemischen und dem Organischen Institut der Justus-Liebig-Universität Gießen durch die Untersuchung der Struktur-Eigenschafts-Beziehung definiert. Maßgeblichen Einfluss auf die elektrochemischen Eigenschaften dieser Verbindungen hat dabei unter anderem der im Elektrolyten vorherrschende pH-Wert. So kann durch dessen Modifizierung das Potential, bei welchem es zum Elektronenübertrag kommt, variiert und die Zelle auf ihre Anwendung in verschiedenen Umgebungen hin optimiert werden. Das Bild des Monats zeigt den Einfluss des pH-Wertes auf die Potentiallagen der elektrochemisch aktiven Spezies in Form von Zyklovoltammogrammen, welche mithilfe einer Dreielektrodenanordnung unter Zuhilfenahme einer Ag/AgCl-Referenzelektrode aufgezeichnet wurden. (Bild eingereicht von Jonas Hofmann.)
April 2016
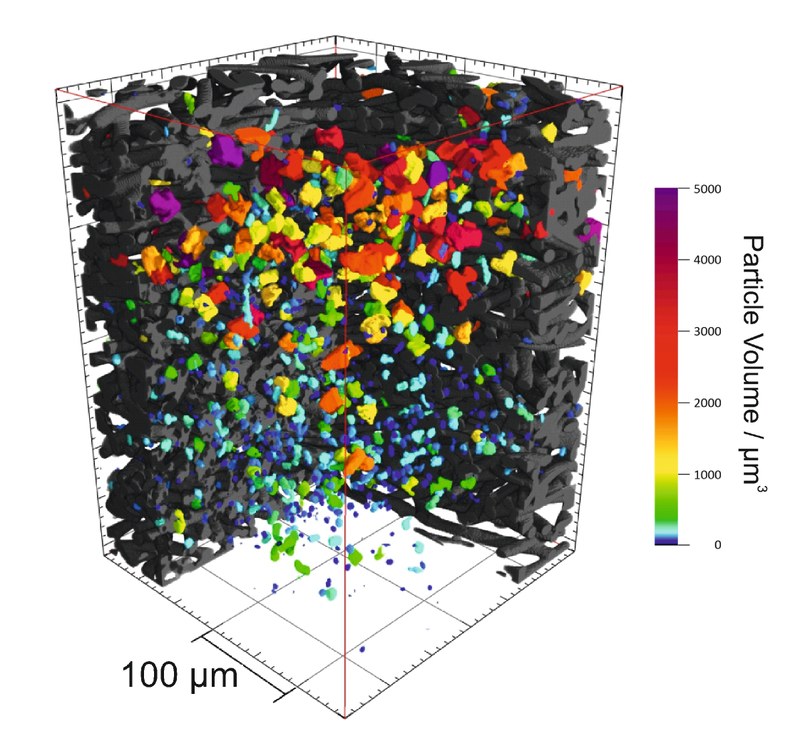
„Durchleuchten“ mit Röntgenstrahlung – Gezeigt ist die Kathode einer Natrium-Sauerstoff-Batterie, in welcher das Entladeprodukt Natrium-Superoxid gespeichert wurde. Typischerweise liegt Natrium-Superoxid in Form kubischer, ca. 20 µm großer Partikel vor und ist während des Betriebs der Batterie nicht direkt analysierbar, da die Partikel vom Batteriegehäuse und weiteren Materialien verdeckt sind. Sichtbar gemacht wurden die Partikel (farbige Abstufung je nach Volumen der Partikel) durch Synchrotron-Röntgen-Transmissions-Tomographie einer voll entladenen Batterie-Kathode. Die Aufnahmen entstanden in Kooperation mit dem Helmholtz-Zentrum Berlin für Materialien und Energie an der Elektronenspeicherringanlage BESSY II, und wurden kürzlich in einer Publikation (http://www.nature.com/articles/srep24288) zusammengetragen.Wiederaufladbare Metall-Sauerstoff-Batterien, wie beispielsweise die Natrium-Sauerstoff-Batterie, gelten als mögliche zukünftige Energiespeicher. In der AG Janek werden Metall-Sauerstoff-Batterien im Rahmen verschiedener Forschungsprojekte wie dem BASF-Forschungsnetzwerk „Elektrochemie und Batterien“ oder dem BMBF-Projekt „BenchBatt“ untersucht. Das Hauptaugenmerk gilt hierbei auf dem tieferen Verständnis und der Verbesserung der zu Grunde liegenden Zelle-Chemie. (Bild eingereicht von Conrad Bender und Daniel Schröder.)