Projekt 5: Wirkstoffscreenings gegen Schistosomen und Leberegel
Hintergrund – DRUID gegen NTDs
Das LOEWE-Zentrum „DRUID“ steht für Novel Drug Targets against Poverty-related and Neglected Tropical Infectious Diseases. Hier arbeiten hessenweit führende Arbeitsgruppen an der Erforschung und Entwicklung von Wirkstoffen und Diagnostika gegen tropische Infektionskrankheiten (siehe https://www.loewe-druid.de/). Unter den Neglected Tropical Diseases (NTDs) verursachen Infektionen mit parasitären Würmern (Helminthen) weltweit die größte gesundheitliche Beeinträchtigung in der Bevölkerung (WHO). Vor dem Hintergrund eines stark limitierten Spektrums antiparasitärer Medikamente und fehlender Impfstoffe machen zusätzlich suboptimale Therapieerfolge und Resistenzen die Entwicklung neuer Wirkstoffe dringend erforderlich.
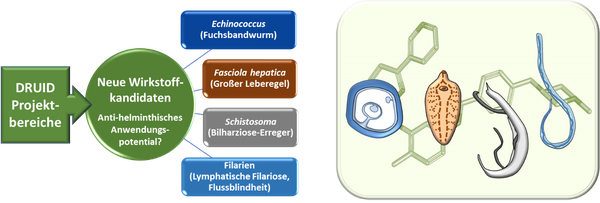
Wie wir neue Wirkstoffkandidaten finden
Im Rahmen unseres Plattform-Projekts in DRUID testen wir neuartige Wirkstoffkandidaten gegen Leberegel und Schistosomen und koordinieren Tests gegen eine Vielzahl weiterer Helminthen in Laboren unserer weltweiten Kooperationspartner. Hervorzuheben sind der Proteinkinaseinhibitor Imatinib und Arylmethylaminosteroide, für die unser Plattform-Projekt ein breites antiparasitäres Wirkspektrum zeigen konnte (Li et al. 2019).
Unsere Arbeitsgruppe leistet zudem Pionierarbeit in der Identifizierung anthelminthisch aktiver Naturstoffe aus Insekten, einer gigantischen und bislang relativ vernachlässigten Bioressource (Gallinger et al. 2022, Kellershohn et al. 2019, Tonk et al. 2020). Dabei unterstützen uns Kooperationspartner des Fraunhofer Instituts für Molekularbiologie und Angewandte Ökologie.
Neben Substanzscreenings charakterisieren wir vielversprechende Wirkstoffziele mit molekularen Methoden. Zu den Zielproteinen gehören GPCRs, Proteinkinasen, Aldehyddehydrogenasen, Autophagie-Proteine und ein Calcium-Kanal (Beutler et al. 2023, Houhou et al. 2019, Mughal et al. 2021 u. 2022). In Kooperation mit der Arbeitsgruppe Spengler kommt AP-MALDI-Massenspektrometrie Imaging zum Einsatz, eine innovative bildgebende Methode, mit deren Hilfe die Aufnahme und Metabolisierung von Wirkstoffen im Parasiten beleuchtet werden kann (Mokosch et al. 2021, Morawietz et al. 2020 u. 2022).
Mit diesem Plattformprojekt schaffen wir die ideale Voraussetzung, Substanzen mit breitem antiparasitären Wirkspektrum zu identifizieren.
Eigene Publikationen zum Thema
Beutler M, Harnischfeger J, Weber MHW, Hahnel SR, Quack T, Blohm A, Ueberall ME, Timm T, Lochnit G, Rennar GA, Gallinger TL, Houhou H, Rahlfs S, Falcone FH, Becker K, Schlitzer M, Haeberlein S, Czermak P, Salzig D, Grevelding CG. Identification and characterisation of the tegument-expressed aldehyde dehydrogenase SmALDH_312 of Schistosoma mansoni, a target of disulfiram. Eur J Med Chem (2023) 251:11517
Gallinger TL, Aboagye SY, Obermann W, Weiss M, Grünweller A, Unverzagt C, Williams DL, Schlitzer M, Haeberlein S. First in silico screening of insect molecules for identification of novel anti-parasitic compounds. Pharmaceuticals (2022) 15(2):119
Houhou H, Puckelwaldt O, Strube C, Haeberlein S. Reference gene analysis and its use for kinase expression profiling in Fasciola hepatica. Sci Rep (2019) 9:15867
Kellershohn J, Thomas L, Grünweller A, Hartmann RK, Hardt M, Vilcinskas A, Grevelding CG, Haeberlein S. Insects in anthelminthics research: Lady beetle-derived harmonine affects survival, reproduction and stem cell proliferation of Schistosoma mansoni. PLoS Negl Trop Dis (2019) 13: e0007240
Li X, Haeberlein S, Zhao L, Mughal MN, Zhu T, Liu L, Fang R, Zhou Y, Zhao J, Grevelding CG, Hu M. The ABL kinase inhibitor Imatinib causes phenotypic changes and lethality in adult Schistosoma japonicum. Parasitol Res (2019) 118: 881-890
Mokosch A, Gerbig S, Grevelding CG, Haeberlein S*, Spengler B*. High-resolution AP-SMALDI MSI as a new tool for drug imaging in Schistosoma mansoni. Anal Bioanal Chem (2021) 413:2755-2766
Morawietz CM, Houhou H, Puckelwaldt O, Hehr L, Dreisbach D, Mokosch A, Roeb E, Roderfeld M, Spengler B*, Haeberlein S*. Targeting kinases in Fasciola hepatica: anthelminthic effects and tissue distribution of selected kinase inhibitors. Front Vet Science (2020). 7:611270
Morawietz CM, Peter Ventura AM, Grevelding CG, Haeberlein S*, Spengler B*. Spatial visualization of drug uptake and distribution in Fasciola hepatica using high-resolution AP-SMALDI mass spectrometry imaging. Parasitol Res (2022) 121(4):1145-1153
Mughal MN, Grevelding CG, Haeberlein S. First characterization of autophagy-related genes in Schistosoma mansoni. Int J Parasitol (2021) S0020-7519:00092-8
Mughal MN, Grevelding CG, Haeberlein S. The anticancer drug imatinib induces autophagy in Schistosoma mansoni. Int J Parasitol (2022) 52(4):211-215
Tonk M, Vilcinskas A, Grevelding, CG, Haeberlein S. Anthelminthic activity of assassin bug venom against the blood fluke Schistosoma mansoni. Antibiotics (2020). 9: 664
